
专家简介:
Bruce Alberts:UCSF教授,美国国家科学院前院长,现任“Science”杂志总编辑,美国总统奥巴马的科学特使。
我很高兴与大家交流,希望大家能去UCSF学习,未来为协和医院做出更好的贡献,成为更好的科学家。我的讲座分为两部分,第一是介绍一些关于DNA的不稳定性及与细胞生物性之间关系的背景;第二是DNA的不稳定性及与肿瘤的关系,以及将来我们怎样利用DNA的修复和变化去治疗肿瘤。
多细胞生物的优势
6亿年前,地球用了10亿年产生了第一个有生命的细胞,又过了20亿年,才有第一个多细胞生物。对多细胞生物来讲,每一个细胞都有其特性,细胞之间也要通过相互作用才能保证整体的功能。尽管细胞之间的合作是非常困难的,需要20亿年来完成,但为避免“肿瘤”细胞过度生长,细胞之间必须学会相互合作。在细胞的整个合作中,信息的传递、互相对话、互相控制非常重要。细胞之间持续地“对话”,每个细胞将它“听到”的信息整合后做出控制其生长的决定,才能完成一个比较可靠的功能。
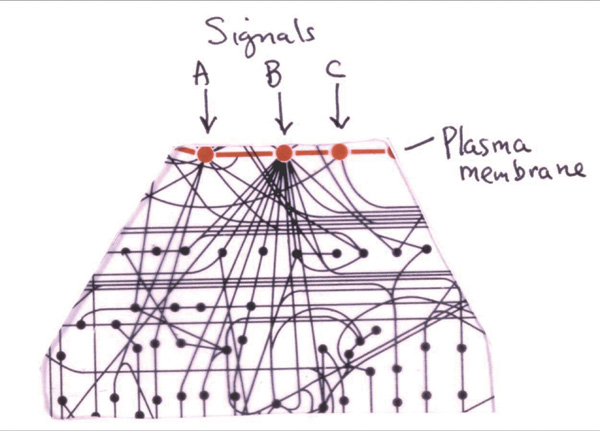
以上这个示意图就是细胞之间怎样进行信号传递功能的。未来的医学或者药物研发,就是要更好地理解整个细胞之间的信号传递通路。每类细胞对信号系统都有不同的解释。可是为什么细胞发生错误的机会非常高,但我们得肿瘤的机会却非常少呢?对于细胞来说,它要了解自身所处的位置,也要了解周围的细胞所处的状态,来决定自己是什么样的状态。大多数细胞是不变的,还有一些细胞会接收一些信号后增殖分化成两个,也有一些会转换成其他的细胞,多数细胞在接受一些信号后变化。
合作与交流——实现信息与资料的最大效用
整个细胞会有很多发生错误的机会,怎样避免发生错误,产生肿瘤是非常重要的。保证DNA的准确性很关键,所以,我们体内有一个DNA聚合酶,它是非常准确的酶系统,能保证DNA的修复过程完整、准确。DNA的修复模板是在另外一条链上开始氨基酸序列复制的;DNA聚合酶的另外一个功能是保证DNA复制过程的准确性,具有自我纠正功能,避免产生肿瘤。对于聚合酶来说,大概会有千分之一的错误率,且错误进入下一个系统时编辑系统会将其去除。
虽然这一系统的准确度非常高,但依然会有一些错误,错误率大概为10-7。这时DNA错配的修复系统就会发挥作用。修复系统中如果发生错配,就会有酶的系统检测它,发现错配后把这一段整个剪切掉(至少99%的错配会被切掉),再合成一个新的。我们体内发生这样错误的机会大概是10-9,我们体内有1014 个细胞,肿瘤的发生机会实际上会非常少,大概在三个生命周期才有一个肿瘤发生机会。这能保证人类的健康吗?
为了回答这个问题,我们可以做一个简单的计算:任何两条基因都可能有50个发生突变的细胞,我们有这么多的基因,每两个就可以出现这么多的错误率,每天体内发生错误的机会非常高。如果从胚胎细胞开始算,突变率会更高。因为人体内细胞在新生和凋亡过程中不断变化的,以最小的细胞分化来算,真正发生的突变要超过细胞分化速度的一百倍,如果考虑到环境因素,像吸烟或接触有害化学物质,比率可能会更高。这就产生了以下结论,第一,在我们整个生命过程里,DNA复制过程中的错误率是10-9;第二,人体中细胞具有控制增殖的自动防故障装置。人体细胞至少有150种以上的DNA修复酶,可避免不同类型的DNA突变和错误机会。修复系统分五类:剪切修复、核苷酸剪切修复、双链重组、不同步的修复系统以及DNA合成修复系统。
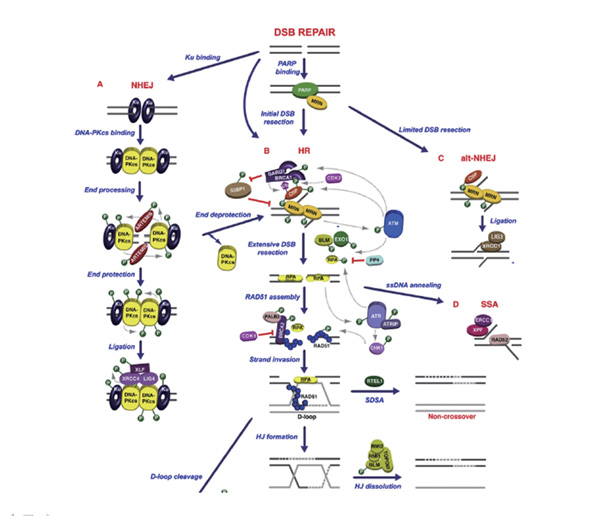
从以上图解可看出,DNA的修复过程是一个非常复杂的过程,至少我们已知的有十几步,每一个修复过程都很复杂。
DNA的不稳定性与肿瘤治疗
接下来跟大家一起讨论前面提到的这些问题和肿瘤治疗之间的关系。首先,肿瘤是不断发展的,这就能解释为什么随着年龄的增加,肿瘤的发生率也会增加。按照每十万人的突变率来看,随着年龄的增加,大概每一个特定的肿瘤需要3个或者4个突变才会发生。那么到底多少个突变会发生肿瘤?
肿瘤领域的知名科学家在2006年发表的一篇文章显示,肿瘤的发展大概需要10到15个突变。也就是说早期出现的DNA修复或它复制的一些错误,可能是产生肿瘤的重要因素,不同的错误会导致不同的疾病。美国西雅图肿瘤研究所在2006年发表的一篇文章也显示,一个细胞肿瘤的突变率大概比正常的突变率高100倍,早期的不稳定性可能会导致细胞突变,产生肿瘤。我们克隆的这些肿瘤最主要还是错配修复系统出了问题,一个正常的染色体出现缺陷是能够进行修复的,肿瘤的染色体会有异常状况。这些研究结果的结论是,DNA不稳定性的异常导致肿瘤不断恶化,而不是突然的出现才导致肿瘤的发生。因此,如果我们知道哪个DNA的修复基因出现了错误,就可以找到新的肿瘤治疗办法。然而,对于肿瘤的发生来说这样的突变太多了,所以很难确定这个细胞。肿瘤细胞的突变率非常高,从遗传学来讲它也是不稳定的,所以如果我们能够知道哪一个修复系统出现了障碍,就能找到一种新的干预手段针对突变的肿瘤细胞进行治疗,而不伤害其周围的正常细胞。
CaseⅠ:DNA的修复过程中,如果不能修复到完全正常,修复就会终止。双链的修复同样如此。如果一个单核苷酸的修复系统出现问题,它就会变成肿瘤细胞,如果有合适的药物,能把修复的细胞杀死,就不会变成一个肿瘤细胞。
CaseⅡ:在乳腺瘤中,BRCA2的缺陷是常见的,我们通过修复它可以进行治疗,把有缺陷的细胞杀掉,这种特异性比普通药物的特异性高一百到一千倍。很多研究者使用RNAi技术,使用这些基因进行治疗,也发现了相似的治疗效果。所以,现在很多制药公司有PARP抑制剂,对任何蛋白的缺陷都可以治疗,而不仅仅是上述提到的这两个缺陷修复。
未来工作
如果对于每一个肿瘤个体都能检测DNA修复异常的基因,则可使PARP抑制剂做到更准确的肿瘤治疗,但目前我们还没有这样的检测方法。所以这是我们未来的一些设想,也是Helleday在2007年的综述里提到,我们未来几十年的挑战,即找到DNA修复异常的机制,针对肿瘤或是通过杀伤这些肿瘤细胞来治愈肿瘤。我们需要对DNA修复系统和DNA损伤系统的各个方面进行全面了解,才能使我们对整个细胞,包括DNA系统的异常有所了解,才能找到更有针对性的治疗办法。
我们需要做的事情很多。首先,要拓宽对DNA的了解,更好地了解一个有机体的工作模式,包括从细菌、果蝇、蠕虫这些简单的生物出发,可能有助于了解生物系统相互工作的机制。第二,现在有很多新的针对肿瘤的特异性药物,包括一期、二期、三期临床实验,比如针对DNA修复系统的一些通路,可能是更有针对性的做法,希望这些方法能够对肿瘤进行更好、更有针对性的治疗。第三,针对其它的靶部位开发新药。因为肿瘤大多数是由于突变率高造成的,最新研究显示,针对肿瘤的修复系统是MSH2和MLH1这两个基因,目前有十几个或二十几个针对不同基因的系统。另外,肿瘤的不稳定性,也就是突变率非常高,我们还需要比较敏感、准确地测定不同肿瘤的突变的检测方法。不同的肿瘤,有的是辅助问题,有些是突变问题,可以针对不同的肿瘤、不同的问题去检测,这也是非常有前景的领域。
总 结
我们未来所面对的最大挑战就是肿瘤的个体化治疗。肿瘤的发生过程非常长,在不同的过程中可能会出现不同的缺陷,我们希望在不同的位置上可以确定病变。中美之间的合作具有非常广阔的前景,我希望不仅是我,在座的年轻科学家、年轻医生也能参与合作。
会场问答
Q:我们发现有些肿瘤经过一段时间的新药物治疗后可能会对这一个药物产生抵抗,你怎么看待这个问题?
A:由于肿瘤不是单一细胞来源,可能是多细胞来源,所以我们的治疗就是需要多种药物同时治疗,某一个肿瘤可能对一些治疗比较敏感,有些比较抵抗。我也提到,现在我们整个治疗策略会有改变,在治疗肿瘤时运用针对不同基因或不同作用机制的药物进行治疗。
Q:未来中国和美国之间在哪些方面会有合作?
A:合作需要非常大的资金支持,过去已经做了很多,包括一些制药公司进行的研究和推出的药物。未来我们还需要一起仔细研究,北京和UCSF之间到底有哪些项目可以合作,我也愿意参加这样的讨论。
















